|
Quais
os avanços no tratamento da epilepsia?
"É
como atirar no escuro e esperar que o alvo seja acertado".
É assim que o neurologista Ley Sander, professor do Departamento
de Epilepsia Clínica e Experimental do University College
London, define o tratamento da epilepsia.
Embora
possa parecer, a definição não é caricatural.
Isto porque, explica ele, não há um tratamento racional
disponível. Terapia "racional", esclarece, é
o tratamento baseado no conhecimento do processo patogênico,
de como a droga o influencia, no fato de que a terapia funciona
seletivamente em um mecanismo e também no conhecimento de
que a escolha do tratamento errado resulta em falha. A epilepsia
é uma condição complexa, muitas vezes mal compreendida,
e as terapias atuais são essencialmente empíricas,
ou seja, "foram formuladas como resultado da experiência
e não sobre o conhecimento do processo patogênico da
epilepsia, o que não quer dizer que elas não sejam
eficientes, mas não são racionais", diz.
Desde
meados da década de 80, sabe-se que o uso de uma única
droga (monoterapia) é suficiente e preferível para
controlar a epilepsia em aproximadamente 70-80% dos pacientes. A
utilização de múltiplas drogas (politerapia),
por outro lado, aumenta os efeitos colaterais dos antiepilépticos.
A incidência desses efeitos é proporcional ao número
de drogas antiepilépticas (DAE) utilizadas, conforme sublinham
Carlos Guerreiro e André Palmini, em Epilepsia, um
compêndio de 34 artigos sobre o assunto (veja
resenha nesta edição). Ainda assim, por diversos
motivos, o recurso a uma segunda droga continua sendo freqüente
no atendimento em saúde, quando a primeira não surte
os efeitos desejados imediatamente.
Muitos
pesquisadores defendem que a monoterapia seja mais explicitamente
indicada, para que a busca pelo tratamento com uma única
droga não se esgotasse nas primeiras tentativas. Entretanto,
a indicação de monoterapia esbarra em outras exigências.
Nos
EUA, por exemplo, Food and Drug Administration (FDA) faz restrições
à concessão da indicação de monoterapia
a drogras antiepilépticas. Em março de 2001, cerca
de 120 especialistas de vários países se reuniram
em um workshop internacional para tentar chegar a um consenso sobre
a maneira de obter aprovação do FDA para a rotulagem
de drogas antiepilépticas como "indicadas para monoterapia".
O problema parece insólito, já que a indicação
de monoterapia parece ser consensual entre os pesquisadores que
tratam da epilepsia e já se tornou uma prática corrente.
Mas ele é mais sutil do que parece, assim como tudo o que
envolve o conceito
de epilepsia.
Acontece
que, para conceder a rotulagem de monoterapia, o FDA exige que se
demonstre diferença de efeito no tratamento com a droga ativa
e um placebo (medicação "de mentira"). Mas
a maioria das DAE recebe aprovação inicial do órgão
através de estudos clínicos do tipo add on,
em que se adiciona a droga que se quer testar ou o placebo a uma
medicação de base, já administrada ao paciente,
e se compara a eficácia do tratamento nos dois casos. O FDA
considera insuficiente essa informação para conceder
a indicação de monoterapia a uma droga, sob a justificativa
de que esse tipo de pesquisa não avalia o efeito individual
da nova DAE. Daí a polêmica que motivou workshop
(promovido pelo Instituto Nacional de Desordens Neurológicas
e Derrames/ Institutos Nacionais de Saúde (NINDS/NIH), Sociedade
Americana de Epilepsia (AES), Cidadãos Unidos pela Pesquisa
em Epilepsia (CURE) e Fundação Epilepsia (EF)) reunindo,
além de pesquisadores epileptologistas e estatísticos,
representantes do FDA e de empresas farmacêuticas. Todos sem
chegar a um consenso.
"O
problema com os testes placebo-controle de monoterapia é
que eles deixam metade dos pacientes sem tomar DAE, portanto expostos
ao risco de crises adicionais e suas conseqüências",
diz o relatório do NINDS sobre o evento. As drogas com indicação
de monoterapia receberam o rótulo através de testes
com pacientes hospitalizados e candidatos a cirurgia, em que a medicação
era suspensa para avaliação. Ou então através
de estudos do tipo "pseudo-placebo", em que se compara
a droga de interesse com uma dose sub-terapêutica de outra
medicação. Tais estudos, no entanto, têm problemas
éticos e científicos, fazendo com que os médicos
e pesquisadores fiquem relutantes em realizá-los. Mesmo as
empresas farmacêuticas têm restrições
em desenvolver esse tipo de estudo.
Na
Europa, as agências européias de regulação
de drogas aceitam testes de equivalência para conceder aprovação
de monoterapia. Uma nova DAE é comparada com uma DAE tradicional,
"comprovadamente eficaz", e caso seja demonstrada sua
equivalência, ela recebe indicação de monoterapia.
A vantagem desse tipo de estudo, diz o NINDS, é que todos
os pacientes recebem medicamento; a desvantagem é que se
pode estar comparando drogas medíocres, já que o teste
é de equivalência e não de superioridade. Segundo
o instituto, o FDA se dispôs a "levar em consideração"
resultados de controles históricos e um grupo de pesquisadores
foi designado para levantar esses dados e ver que evidências
positivas existem.
Politerapia "racional"
Se,
por um lado, a monoterapia é hoje indicada na maior parte
dos casos, por outro, ela convive com uma estratégia que
muitos chamam de "politerapia racional", que consiste
em combinar várias DAE com diferentes mecanismos de ação,
para tentar reduzir os efeitos colaterais, ao mesmo tempo que busca-se
obter maior eficácia terapêutica e diminuir a interação
com outras drogas. Essa abordagem terapêutica surgiu com o
desenvolvimento da pesquisa sobre os diversos tipos de epilepsia
e a introdução da classificação das
crises e síndromes epilépticas pela Liga Internacional
Contra a Epilepsia (ILAE), apontando indicações mais
precisas sobre a DAE adequada para cada tipo de epilepsia (veja
tabela abaixo).
Tipos
de crises, síndromes e drogas antiepilépticas
|
Tipos de crises |
| Crise
parcial com ou sem generalizacão |
Ausência |
C.
Miociônicas |
CTCG
(primárias) |
| Carbamazepina |
Valproato |
Valproato |
Valproato |
| Valproato |
Etossuxicimida |
Benzodiazepínicos |
Carbamazepina |
| Fenitoína |
Lamotrigina |
Primidona |
Fenitoína |
| Fenobarbital |
Benzodiazepínicos |
Lamotrigina |
Fenobarbital |
| Primidona |
Topiramato |
Topiramato |
Fenitoína |
| Benzodiazepínicos |
|
|
Oxcarbazepina |
| Oxcarbazepina |
|
|
Lamotrigina |
| Lamotrigina |
|
|
Topiramato |
| Vigabatrina |
|
|
|
| Topiramato |
|
|
|
| Gabapentina |
|
|
|
|
Síndromes |
| S. West |
S. Lennox-Gastaut |
Epilepsia Fotossensível |
|
Vigabatrina |
Valproato |
Valproato |
|
Esteróides |
Benzodiazepínicos |
Benzodiazepínicos |
|
Valproato |
Carbamazepina |
Lamotrigina |
|
Benzodiazepínicos |
Vigabatrina |
|
|
|
Lamotrigina |
|
|
|
Oxcarbazepina |
|
|
|
Topiramato |
|
Adaptado
de Guerreiro et al. (2000), Epilepsia, São
Paulo: Lemos Editorial
"Teoricamente",
como notam Guerreiro e Palmini, "esses conhecimentos permitiriam
uma politerapia mais racional". Entretanto, os avanços
conseguidos com as novas DAE são limitados e é difícil
comprovar um aumento de sua eficácia em relação
às drogas tradicionais. De fato, as várias estratégias
de tratamento da epilepsia ao longo de décadas ilustram,
segundo eles, "a influência de um certo 'modismo' na
prescrição médica, refletindo provavelmente
influências de diversas origens, além do simples conhecimento
sobre a condição e sobre as DAE".
O problema,
segundo Ley Sander, é que há resistência em
se reconhecer a natureza essencialmente empírica do tratamento
da epilepsia e o termo "terapia racional" acaba aparecendo
com freqüência. No entanto, diz, "a escolha de uma
DAE é influenciada principalmente pelo tipo de crise, independentemente
da etiologia, e freqüentemente por escolha pessoal [do médico].
A prática clínica é baseada mais no dogma do
que no conhecimento científico". Exemplos de terapia
racional são: o tratamento do hipotiroidismo e o da hipertensão,
por drogas que agem sobre a angiotensina. No caso da epilepsia,
contudo, muitas conclusões sobre as DAE são extrapolações
de modelos animais, que nunca foram validados e cuja relevância
é difícil determinar, afirma o pesquisador.
Novas drogas
O objetivo da pesquisa sobre novas DAE é chegar a medicamentos
mais eficazes, específicos para cada tipo de epilepsia, e
com menos efeitos colaterais. Muitos medicamentos têm sido
testados nos últimos anos e cerca de dez estão disponíveis
comercialmente, mas eles só são indicados quando o
tratamento com as drogas tradicionais não funciona. Isto
porque seus mecanismos de ação e efeitos colaterais
ainda não são bem conhecidos, embora elas tenham sido
baseadas no conhecimento mais racional da fisiologia das crises
epilépticas, ao contrário das drogas tradicionais.
"Os medicamentos tradicionais ou de primeira linha foram achados
praticamente ao acaso", explica Li Li Min, neurologista e professor
da Faculdade de Ciências Médicas da Unicamp. O valproato,
por exemplo, era o solvente usado para testar várias DAE
que apresentavam propriedades anticonvulsivantes e os pesquisadores
acabaram observando que ele era o responsável pela ação
antiepiléptica (veja artigo nesta edição).
|
Drogas
tradicionais
de primeira linha
|
Fenobarbital
Fenitoína
Carbamazepina
Valproato |
|
Novas
drogas
|
Lamotrigina
Oxcarbamazepina
Topiramato
Gabapentina
Remacemida
Tiabagina
Levetiracetam
Zonisamida
Vigabatrina (está fora
do mercado por induzir
cegueira central)
Felbamato (tem uso restrito,
por causa de hepatoxicidade
e aplasia de medula óssea) |
Em
relação às novas drogas, há três
estratégias básicas de pesquisa, como apontam Carlos
e Marilissa Guerreiro, no livro Epilepsia:
- Drogas que inibem a excitação
- Drogas que aumentam a inibição
- Drogas que modificam a excitabilidade celular por meio de interferência
com canais iônicos
Hoje,
os esforços estão concentrados nas seguintes áreas,
diz Ley Sander:
- Identificar novos alvos funcionais na epilepsia, que possam levar
a modificações da condição ou a drogas
antiepileptogênicas ao invés de drogas contra crises
- Encontrar novas formas de levar as drogas diretamente ao foco
epileptogênico
- Atentar para possíveis alvos imunológicos
- Estabelecer o papel potencial das proteínas transportadoras
de drogas no desenvolvimento da epilepsia crônica
- Identificar novos sistemas de neurotransmissão, já
que está claro que o funcionamento do cérebro não
é simplesmente condicionado pelo esquema excitação/inibição
- Explorar o potencial da farmacogenética para identificar
respostas em pacientes de risco
Uma
possível característica importante das novas drogas
antiepilépticas seriam suas propriedades neuroprotetoras.
Alguns estudos buscam confirmá-la. Um pesquisa feita por
M. Gruenthal, M. Zimmerman e P. Googins, da Universidade de Louisville
(KY-USA), mostrou uma associação significativa do
topiramato com a redução dos danos ao hipocampo neuronal
em animais. "Essa 'proteção' é importante,
pois a recorrência de crises tem sido relacionada ao dano
neuronal e, ao longo do tempo, a um declínio da memória,
principalmente em epilepsias de difícil controle como a do
lobo temporal", comenta Li.
Para
Carlos e Marilissa Guerreiro, o papel das novas drogas no tratamento
da epilepsia ainda não está bem definido. Os principais
problemas a serem enfrentados são o alto custo dos medicamentos,
sua segurança e tolerabilidade (ainda não muito bem
definidos) e sua própria eficácia. "Poucos pacientes
ficam completamente livres das crises epilépticas (...);
a redução de dez para duas crises semanais pode não
refletir na melhora da qualidade de vida do paciente", avaliam.
Custos
elevados
O elevado custo das novas DAE é uma preocupação
em todos os países, mas principalmente nos países
em desenvolvimento. Diversas pesquisas têm sido feitas para
avaliar o seu impacto no custo geral do tratamento da epilepsia
e os resultados mostram que a diferença é grande em
relação ao uso de DAE tradicionais. Um estudo de D.
Galdames e S. Erazo feito com pacientes de um hospital em Santiago
(Chile) mostrou que o custo médio anual do tratamento usando
drogas convencionais era de US$ 65 por paciente, enquanto que o
com novas drogas era de US$ 655. As primeiras eram usadas por 96%
dos pacientes e representavam 70,4% do custo total. As novas DAE
eram usadas por 3.8% dos pacientes e representavam 29,4% do custo
total. Eles concluem que há necessidade de se aumentar o
orçamento destinado às DAE e, simultaneamente, baixar
o preço das novas DAE. O estudo foi apresentado no Congresso
da Liga Internacional Contra a Epilepsia (ILAE) e do Escritório
Internacional para Epilepsia (IBE).
Outros
dois estudos apresentados nesse Congresso,
salientam o peso dos medicamentos nos custos do tratamento da epilepsia.
S. Gonzales-Pal, Y. Valor Carmona e J. C. Prego Regalado, do Hospital
Psiquiátrico de Havana (Cuba), chegaram ao cálculo
de US$ 392/ano gastos por paciente. Destes, US$ 103 são para
medicação, no caso de pacientes tratados com uma única
DAE, e US$ 129 para os tratados com mais de uma DAE. O maior custo,
concluem, está em misturar diversas DAE e poderia ser reduzido,
ajustando-se o tratamento para torná-lo mais econômico.
Em
uma meta-análise (procedimento que permite comparar dados
de pesquisas que utilizaram metodologias diferentes), levando em
consideração artigos sobre o custo do tratamento da
epilepsia em alguns países, publicados entre 1966 e 2000,
I. Kotsopoulos, S. Evers, A. Ament e M. de Krom, do Hospital Universitário
de Maastrich (Holanda), observaram que a proporção
dos gastos nacionais em saúde com a epilepsia variam entre
0,12% e 1,12%, dependendo principalmente dos gastos com drogas e
gastos hospitalares. No Brasil, não temos dados precisos
sobre os gastos totais do governo com epilepsia é difícil
fazer uma comparação com os dados dos autores (veja,
nesta edição, as reportagens sobre epidemiologia
da epilepsia e política de saúde),
porém a variação encontrada e os fatores que
a condicionam, mostram a importância de se estudar o tema.
Terapias
alternativas
Quando o tratamento medicamentoso da epilepsia não funciona,
o que ocorre em cerca de 15% dos casos (veja gráfico abaixo),
algumas alternativas existem: cirurgia, dieta cetogênica e
estimulador do nervo vago, principalmente. A primeira é,
inclusive, indicada independentemente do tratamento medicamentoso,
em casos específicos.
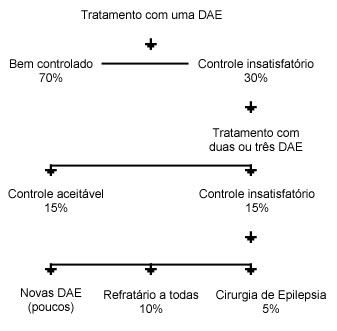
Controle
esperado de epilepsias recém-diagnosticadas
Adaptado
de Guerreiro et al. (2000), Epilepsia, São
Paulo: Lemos Editorial
Dennis
Spencer, neurocirurgião da Universidade de Yale, agraciado
com uma bolsa de US$ 7 milhões ( veja
notícia) para pesquisa em cirurgia da epilepsia, explica,
em entrevista a ComCiência, que no caso de algumas epilepsias,
como o do lobo temporal, a cirurgia vem sendo crescentemente considerada
para aplicação, mesmo em pacientes controlados com
DAE, pois nestes casos o controle das crises geralmente requer níveis
tóxicos da droga. Seu projeto de pesquisa consiste em utilizar
modernas técnicas de imagem (por ressonância magnética)
e tentar combinar imagens químicas, funcionais e anatômicas
no mesmo espaço, para em seguida correlacioná-las
com eletroencefalograma e mapeamento funcional do cérebro.
Com isso, os pesquisadores esperam localizar com maior precisão
os focos das crises epilépticas para remoção,
resguardando ao máximo as funções cognitivas
do paciente (veja também artigo sobre o Projeto
Cinapce, nesta edição).
Quanto
ao estimulador do nervo vago, ele é uma espécie de
marca-passo, implantado no paciente com a função de
diminuir a hiperexcitação dos neurônios, dessincronizando-os
(na crise epiléptica, o que ocorre é uma atividade
intensa e sincronizada dos neurônios). Segundo Ley Sander,
o estimulador leva a uma melhora de cerca de 50% nas crises, em
cerca de 30% dos pacientes em que é implantado. Para ele,
o estimulador do nervo vago é, na melhor das hipóteses,
um tratamento paliativo. O custo de implantação na
Inglaterra é de 8.500 libras esterlinas por procedimento.
"Espero que o estimulador seja em breve só uma má
lembrança", diz o pesquisador.
Já
a dieta cetogênica, é um tratamento que vem sendo pesquisado,
mas ainda não tem eficácia comprovada. Um estudo da
Escola de Medicina da Universidade Johns Hopkins (EUA), divulgado
recentemente pela New
Scientist, mostrou uma melhora significativa em crianças
que utilizaram a dieta, até seis anos após a sua suspensão
(depois de terem ficado cerca de um ano fazendo-a). Um quarto das
150 crianças tratadas ficaram livres das crises e mais da
metade apresentou uma diminuição de 50% na freqüência
de crises. Mas os pesquisadores ainda não sabem exatamente
como a dieta cetogênica reduz as crises. "Há muitos
cientistas trabalhando sobre o assunto, mas eles ainda não
chegaram sequer à questão de como a dieta faz efeito
muito tempo depois de ter sido suspensa", afirma John Freeman,
pesquisador da equipe responsável pelo estudo.
Outras
frentes de pesquisa vêm sendo abertas sobre a epilepsia. Por
exemplo, uso do ácido ascórbico (vitamina C) para
potencializar a passagem das drogas antiepilépticas para
o sistema nervoso central (veja
notícia da New Scientist sobre o trabalho da equipe de
Stefano Manfredini, da Universidade de Ferrara). Por enquanto, elas
estão em fase laboratorial, a maioria em estágio pré-clínico
(testes apenas com animais), mas abrem a possibilidade de que a
epilepsia venha a ser tratada de maneira mais específica
e eficaz no futuro.
(MM)
|