Por Graciele Almeida de Oliveira e Sophia La Banca de Oliveira
Recentemente proposto para diagnóstico de câncer e de doenças virais, como a dengue e o zika, o sistema CRISPR-cas está começando a ser usado em testes clínicos em humanos
Três trabalhos publicados no final do mês de abril mostraram que sistemas chamados Sherlock e Detectr podem se tornar ferramentas baratas e eficazes no diagnóstico da infecção pelo vírus zika. Esses sistemas se baseiam numa tecnologia chamada CRISPR-Cas.
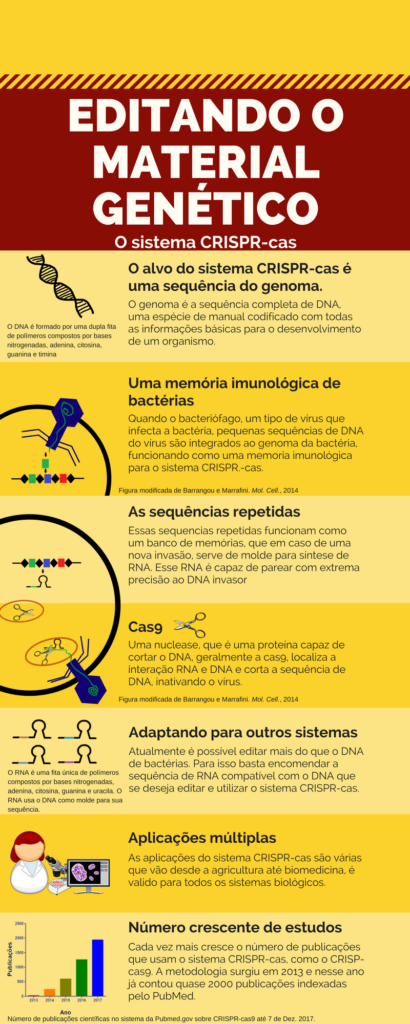
O CRISPR-Cas é uma ferramenta de alta precisão para alterar o genoma – que é uma espécie de manual codificado com as informações básicas para o desenvolvimento de um organismo. Anunciado há quatro anos como uma tecnologia revolucionária, levou cerca de duas décadas para ser desenvolvido, com esforços de vários pesquisadores, de diferentes países.
O espanhol Francisco Mujica foi o primeiro a notar as múltiplas cópias de sequências no material genético de bactérias, as quais deu o nome de clustered regularly interspaced palindromic repeats (CRISPR, em português: repetições palíndromas de clusters regularmente espaçados).
Após vários estudos, o pesquisador descobriu que CRISPR era, na verdade, uma resposta adaptativa do sistema imunológico desses microrganismos. No caso de uma infecção viral, por exemplo, o organismo faz uma cópia de uma sequência de DNA associada ao do vírus. Isso serve como instrução para proteger de uma reinfecção.
Depois, com a descoberta da Cas9, proteína capaz de cortar o DNA em uma posição bem específica, a dupla CRISPR-cas9 tornou-se uma opção para a edição de DNA.
O otimismo dos pesquisadores com a ferramenta é grande. Isso porque outras formas de manipulação do material genético já eram utilizadas, mas com menos eficácia. “Antes havia o silenciamento do gene, mas ainda com uma expressão, pequena, mas muitas vezes suficiente para que o gene se expressasse. Caía de 100% para 80%, por exemplo. Agora vemos o nocaute, ou seja, 0. Isso é muito importante. E com o CRISPR é extremamente fácil, barato e eficiente. Antes era difícil, caro e ineficiente”, compara Clarissa Rocha, pesquisadora do Laboratório de Reparo do DNA, no Instituto de Biologia da USP.
Apesar de recente – para os tempos médios do desenvolvimento científico – a ferramenta de edição é amplamente usada em pesquisas, com possibilidades de geração de modelos celulares para diversos estudos, screening genético e mesmo correção de desordens genéticas. Desde 2016 há aprovação para uso em testes clínicos, como o em andamento no National Institute of Health dos Estados Unidos, para tratamento de câncer de células T, ligada à imunidade.
Uso terapêutico
Clarissa Rocha estuda genes associados à resistência de tratamento em tumores de glioma, uma forma agressiva de câncer. Por meio dessa técnica, ela foi capaz de identificar, pela primeira vez, genes associados à resistência a um agente quimioterápico – ou seja, quando o medicamento não age como deveria.
No Laboratório Nacional de Células Tronco Embrionárias, sob a coordenação da pesquisadora Lygia da Veiga Pereira Carramaschi, outros usos estão sendo testados com ajuda da ferramenta. “Escolhemos o CRISPR/Cas9 por ser uma técnica que requer um conhecimento de biologia molecular relativamente simples em comparação às outras técnicas”, diz Juliana Borsoi Sant’Ana, doutoranda no laboratório. O objetivo do estudo de Sant’Ana é encontrar um modelo in vitro para estudar as manifestações cardíacas em pacientes com Síndrome de Marfan, uma doença genética hereditária que causa uma desordem no tecido conjuntivo. As manifestações mais comuns são as esqueléticas, como deformidade torácica, cardíacas, problema no funcionamento das válvulas cardíacas e oculares, como miopia e luxação do cristalino.
“O estudo possivelmente vai permitir que sejam desenvolvidos novos métodos terapêuticos para melhorar a qualidade de vida dos pacientes, talvez com fármacos mais específicos e eficientes, por exemplo”, explica Sant’Ana.
Implicações éticas
Se o uso da tecnologia CRISPR-Cas para fins médicos e terapêuticos é desejado, sua possibilidade para introduzir melhoramentos genéticos gera discussão. Isso porque os genes editados pela ferramenta podem ser herdados pelas gerações futuras, como no caso de manipulação em embriões e gametas. As controvérsias ganharam força em 2015, quando um grupo de cientistas publicou o primeiro artigo com resultados em embriões pré-implantados usando esse tipo de manipulação, meses depois que outro grupo de pesquisadores renomados pediu uma moratória nesse tipo de pesquisa.
O genoma humano foi declarado patrimônio da humanidade pela Unesco em 1997, com decisão sancionada pela Assembleia Geral da ONU, em 1998. No entanto, de acordo com a professora da Universidade Estadual de Londrina, Nilza Maria Diniz, especializada em genética e bioética, a declaração não é levada em conta pelos pesquisadores. “Isso foi esquecido. A ciência atropela as questões morais”.
Com as novas possibilidades, surge a pergunta se pais podem decidir por alterações genéticas nos filhos. Essa questão é, muitas vezes, minimizada por bioeticistas, uma vez que o questionamento já foi feito em outros momentos de avanço da tecnologia. Em um texto publicado no Journal of Medicine and Philosophy, Ray Moseley afirma que “os efeitos de manipulações na linhagem germinativa das gerações futuras não são eticamente diferentes de qualquer outra decisão humana que afete as gerações futuras”. Nilza Diniz também aponta que outras tecnologias de reprodução assistida já são utilizadas dessa forma. “Na proveta há vários tipos de manipulação de seleção”.
Se, por um lado, há grupos que defendem o uso livre de dessa e de outras tecnologias para superar todas as limitações biológicas e cognitivas do ser humano, outros comparam a ideia de melhoramento genético à eugenia. Diante destas questões, a comunidade científica tem adotado uma posição mais cautelosa, como exemplificado pelo relatório divulgado em 2017 pela Academia Nacional de Ciências dos Estados Unidos.
Na decisão sobre o uso ou não de métodos de edição do genoma humano é preciso também levar em consideração o acesso desigual a esse tipo de tecnologia. “Há diferença entre pobres e ricos, entre quem tem acesso à tecnociência e quem não tem, e aprofundaríamos ainda mais essa diferença”, pondera Nilza.
No Brasil pesquisas com embriões humanos devem ser aprovadas previamente por um Comitê de Ética em Pesquisa e pela Comissão Nacional de Ética em Pesquisa, mas ainda não existe regulamentação específica voltada para pesquisas envolvendo a edição de genoma de embriões humanos, nem o uso da tecnologia CRISPR-Cas.
Graciele Almeida de Oliveira é bacharel em química (USP), doutora em ciências – bioquímica, cursa Licenciatura em Educomunicação (USP) e é aluna da pós-graduação em jornalismo científico pelo Labjor/Unicamp.
Sophia La Banca de Oliveira é formada em ciências farmacêuticas (UFPR), mestre em bioquímica (USP) e doutora em psicobiologia (Unifesp). É aluna do curso de especialização em jornalismo científico Labjor/Unicamp.
